코로나19 치료제·백신의 사용허가를 위한 3중 자문 절차가 생긴다.
식품의약품안전처는 14일 코로나19 치료제·백신 허가심사를 위한 외부 전문가 자문 계획에 대해 설명했다.
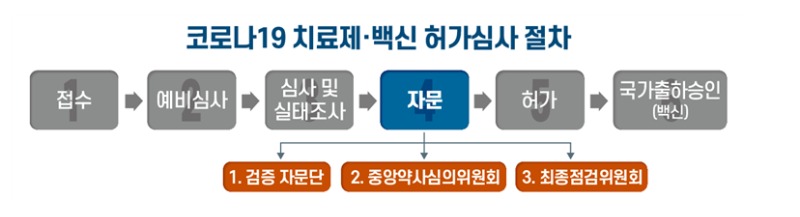
식약처에 따르면 코로나19의 치료제·백신의 검증을 위해 본래 약사법에 따라 운영하는 ‘중앙약사심의위원회’ 이외에도 ‘코로나19치료제/백신 안정성·효과성 검증 자문단’(이하 검증자문단)과 ‘최종점검위원회를 추가해 총 3중의 자문 절차를 거치겠다고 밝혔다.
‘검증자문단’은 다양한 전문가들로부터 임상·비임상·품질 등 분야에 대한 자문의견을 수렴하고, ‘중앙약사심의위원회’는 신청 품목의 안정성, 효과성, 허가 시 고려할 사항 등을 자문한다. 마지막으로 ‘최종점검위원회는’ 내·외부 전문가가 공동으로 참여해 앞서 두 개의 결과를 토대로 최종점검을 실시한다.
식약처 관계자는 “다양한 전문가 의견을 수렴해 객관성과 투명성을 확보하고 철저한 허가·심사가 이뤄질 수 있도록 노력하겠다”고 말했다.
한편 셀트리온의 코로나19 치료제 ‘렉키로나주’는 17일 ‘검증자문단’ 회의를 거쳐, 18일 결과가 나올 예정이다.
<저작권자 ⓒ 한국건강신문, 무단 전재 및 재배포 금지>
- 이정희 기자
[email protected] - 다른기사보기




